2025年1月15日,bat365在线唯一官网登录官网尹燕霞和骆静老师在期刊Analytical and Bioanalytical Chemistry(中科院化学大类2区,JCR Q1)发表“Study of the interaction between alkaline phosphatase and biomacromolecule substrates”论文。
在bat365官网的分子生物学和生物化学实验的本科教学中,大肠杆菌碱性磷酸酶基因(phoA)的克隆和碱性磷酸酶蛋白(alkaline phosphatase,ALP)表达、纯化及其酶学功能研究是核心教学内容。以往针对ALP的酶学研究主要是使用无机小分子—对硝基苯酚磷酸盐(pNPP)作为底物。在科学研究中,ALP通常用于分子克隆,比如去除DNA或RNA的5’末端磷酸基团;防止载体的自环化连接等;还可以用于磷蛋白的去磷酸作用等等。然而,目前还没有关于ALP与这些生物大分子之间相互作用的报告。
微量热泳动技术(MST)和等温滴定量热法(ITC)是常用的测定大分子相互作用的实验方法,但在实际测定中野生型ALP是不能使用的,因为酶促反应会干扰亲和力的测定。我们表达纯化了带有his-tag的S102L ALP,该突变体保留了酶与底物的亲和力,但由于没有102位丝氨酸的亲核基团,丧失了其对底物的催化活力。我们使用RED-Tris-NTA染料 标记S102L ALP,利用MST测定了其与两种双链DNA(double strand DNA,dsDNA)的亲和力;还利用ITC和GST pull-down技术测定了S102L ALP与磷蛋白β-casein的相互作用。

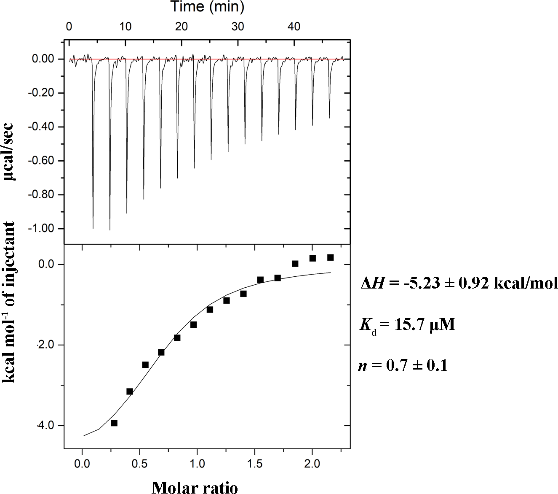
从化学结构的角度来看,酶和底物识别的基础是亲和力和特异性。亲和力代表了酶和底物之间相互作用产生的能量,从而反映了它们的稳定性。我们发现S102L ALP对dsDNA和β-酪蛋白均具有很强的亲和力,这也是ALP作为非特异性酶,与底物识别的关键所在。同时我们还发现底物磷酸单酯(ROP)中的R基团的特性对于亲和力有一定的影响,ALP对于线性dsDNA的亲和力要高于球形的蛋白质大分子。综上所述,我们从亲和性的角度解释了ALP与生物大分子底物相互作用的关键因素,为更好地理解碱性磷酸酶提供了指导。
分子生物学技术日新月异,在教学实践中及时融入新技术是进行教学改革和提高人才培养质量的重要目标。本研究提出的科学问题来自于教学需求,并将解决问题的方案应用于教学实践中,形成了教学质量的提升。bat365官网登录入口体育2022级硕士生李雅楠为本文的第一作者,文中的ALP晶体学数据和蛋白纯化技术得到了杨冬和佟丽老师的大力帮助。尹燕霞和骆静老师是本文的共同通讯作者,本研究得到了bat365官网登录入口体育教学建设与改革项目的大力支持。
原文链接:https://link.springer.com/article/10.1007/s00216-025-05740-3